US-Arzneimittelbehörde erteilt Coronavirus-Schnelltest Zulassung
Ein US-amerikanisches Unternehmen hat von der FDA eine Zulassung für einen Coronavirus-Schnelltest erhalten, der in wenigen Stunden Ergebnisse liefern soll.
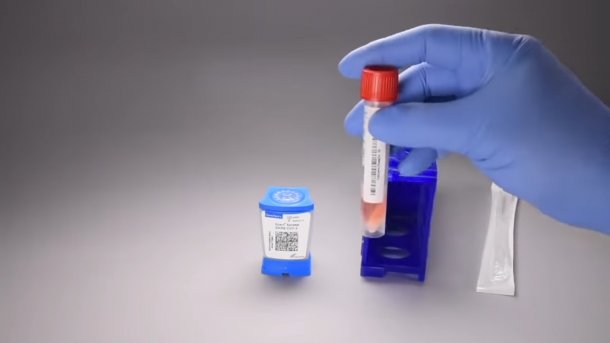
(Bild: Cepheid / Screenshot aus Video)
Die US-amerikanische Lebensmittel- und Arzneimittelbehörde FDA (Food an Drug Administration) hat einem Schnelltest auf Erkennung des Coronavirus SARS-CoV-2 (das die Lungenkrankheit COVID-19 hervorrufen kann) eine Notfallzulassung erteilt. Der Hersteller, das kalifornische Unternehmen Cepheid, gibt die Erkennungszeit mit ca. 45 Minuten an. Damit wären Testergebnisse laut FDA binnen Stunden verfügbar, statt wie derzeit nach 24 bis 48 Stunden oder teils bis zu vier Tagen.
Test vor Ort in wenigen Stunden
Cepheid sieht seinen "Xpert Xpress SARS-CoV-2" genannten Test in erster Linie zur Unterstützung von Kliniken vor, weil die Tests vor Ort stattfinden könnten. Die Probe wird im Analysegerät "GeneXpert" des Herstellers verarbeitet, das auch für die Prüfung anderer Infektionskrankheit wie Tuberkulose und HIV geeignet ist. Bislang müssen Proben meist an ein Labor geschickt werden. Cepheid gibt die Zahl der in den USA verfügbaren "GeneXpert"-Analysegeräte mit knapp 5000 an, die sich zum größten Teil in Krankenhäusern befänden; weltweit sollen es über 23.000 sein. Die Auslieferung der Testkits soll am 30. März beginnen, schreibt die FDA in ihrer Mitteilung. Über mögliche Zulassungen in anderen Ländern macht der Hersteller zurzeit noch keine Angaben.
c
Der Hersteller bezeichnet sein Testverfahren als qualitativ vergleichbar mit bestehenden Labortests. Der Abstrich des Patienten wird in einem Röhrchen vermischt und dann mit einer mitgelieferten Pipette in eine Testkartusche gefüllt. Diese wird anschließend in das "GeneXpert"-Analysegerät gesteckt, das der Hersteller in verschiedenen Größen anbietet.
(tiw)